Саркома у детей прогноз

Общие сведения
Данный недуг обладает чрезвычайной злокачественностью, характеризуется бурным течением и способностью быстро давать метастазы.
Рак кости может развиться у людей в любом возрасте, однако чаще всего возникает в период полового созревания у детей и подростов в возрасте от 10 до 20 лет, а также у очень пожилых людей. Обычно патология наблюдается у мужчин, они страдают этим недугом два раза чаще женщин. Излюбленное месторасположение опухоли — цилиндрические или трехгранные кости, поэтому нижние конечности повреждаются чаще, чем верхние.
Существует мнение, что рак кости развивается вследствие длительных воспалительных процессов, например, хронического остеомиелита.
Поэтому чаще всего поражаются следующие кости:
- бедренная;
- большеберцовая;
- плечевая;
- тазовая;
- малоберцовая;
- плечевая;
- локтевая.
Лучевая кость и надколенники достаточно редко поражаются остеосаркомой. Поражение черепа происходит чаще всего в детском возрасте, а также в старческом возрасте в результате осложненной остедистрофии.
Саркома Юинга – злокачественная опухоль костей, характеризующаяся быстрым ростом и ранним появлением метастазов. Обычно развивается у детей, подростков и лиц молодого возраста. Сопровождается болями и местными изменениями мягких тканей (отек, гиперемия, гипертермия). На поздних стадиях опухоль становится заметна при осмотре и пальпации. Лечение осуществляется врачом-онкологом, включает в себя оперативное удаление новообразования, химио- и лучевую терапию.
Саркома Юинга – вторая по частоте злокачественная опухоль костной ткани, возникающая в детском возрасте, составляет от 10 до 15% от общего числа злокачественных новообразований костей. У взрослых старше 30 и детей младше 5 лет встречается редко. Наибольшее количество случаев заболевания приходится на возраст от 10 до 15 лет. Мальчики болеют чаще девочек, европеоиды – чаще представителей негроидной и монголоидной расы.
В отдельных случаях первичное новообразование при этом заболевании возникает в мягких тканях, а не в костях. Такая форма заболевания называется экстраоссальной (внекостной) саркомой Юинга. Кроме того, существуют сходные по характеру и структуре агрессивные злокачественные опухоли, относящиеся к группе так называемых опухолей семейства саркомы Юинга. В эту группу, кроме внекостной и костной саркомы относят ПНЭО (периферические примитивные нейроэктодермальные опухоли). Внекостные формы и ПНЭО в сумме составляют около 15% от всего числа случаев саркомы Юинга.
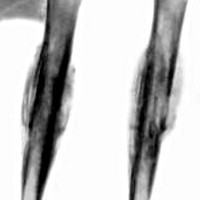
Саркома Юинга

Саркомы, среди общего количества злокачественных новообразований, диагностируются лишь в 5% случаев. Они отличаются агрессивным течением болезни и высокой летальностью. Опасность саркомы еще и в том, что она характерная для пациентов до 30 лет, часто ее болеют дети. Возникновение заболевания именно в детском возрасте обусловлено тем, что активное развитие соединительнотканных структур происходит в детском возрасте, а именно такого рода тканях и образуется опухоль.
Ведущие клиники в Израиле
Учитывая серьезность заболевания и высокий риск смертельного исхода, возникает вопрос о заразности такой болезни. К счастью, такое заболевание не заразно, Саркомой можно заболеть из-за нарушения генетического кода, хромосомных трансформаций.
Диагностирование саркомы при наличии ВИЧ считается геморрагическим саркоматозом и называется ангиосаркома или саркома Капоши. Ее характерные признаки – изъявление кожи и слизистых, а возникает она в результате попадания герпеса 8 типа посредством лимфы, крови (иных секреций кожи и слюны заболевшего) или посредством полового контакта.
Причины заболевания и факторы риска
Причины развития саркомы Юинга в настоящее время точно не установлены. Однако ряд исследователей в сфере современной онкологии считает, что определенную роль в возникновении этого заболевания играет наследственная предрасположенность. Примерно в 40% случаев выявляется связь с предшествующей травмой.
Существуют данные, свидетельствующие о повышении вероятности развития болезни у пациентов с некоторыми разновидностями скелетных аномалий (аневризмальной костной кистой, энхондромой и др.), а также нарушениями внутриутробного развития мочеполовой системы (редупликацией почечной системы, гипоспадиями). Какой-либо связи с воздействием ионизирующей радиации не установлено.
Данный вид опухоли имеет некую связь с быстрым ростом костей. Поэтому остеосаркома поражает преимущественно детей высокого роста, рост которых выше пределов возрастной нормы. Другими словами, недуг развивается у детей очень высокого роста, поскольку остеосаркома поражает быстро растущие части опорно — двигательной системы.
Одной из причин развития данного недуга может быть радиация, которой по какой — либо причине подвергаются дети и подростки. Именно этот факт может стать причинной гормональных нарушений и ослабить организм ребенка. Однако дети или подростки заболевают не сразу. Промежуток между воздействием радиации и развитием недуга может быть в среднем около 10 — 15 лет.
Развитие заболевания наблюдается у лиц, которые имеют в анамнезе доброкачественные опухоли (остеохондромы).
Развитие опухоли кости может случиться в результате травмы. Получается так, что травма привлекает внимание специалиста и заставляет провести инструментальные исследования (рентген и МРТ), в ходе которых диагностируется недуг. Болезнь Педжета может быть точкой отсчета остеосаркомы, нередко с множественным поражением кости.
Остеосаркома наблюдается у лиц, которые раннее переболели ретинобластомой (опухолью, имеющей наследственную этиологию). При этом 50% вторичных опухолей уже приходятся на остеосаркому, а при обоих заболеваниях наблюдаются генетические изменения в хромосомах.
Точные причины возникновения сарком не установлены, но есть связь между присутствием некоторых факторов и образованием опухоли:
- наследственность (генетическая предрасположенность, присутствие патологий хромосомного порядка);
- радиационное излучение;
- влияние канцерогенных веществ;
- долгое нахождение на открытом солнце (посещение солярия);
- вирусы (папилломавирус, герпесвирус, вирус Эпштейн-Барра, ВИЧ);
- работа на вредном производстве;
- сбои иммунного характера, которые могут вызвать развитие аутоиммунных патологий;
- присутствие предраковых состояний;
- проведение иммуносупрессивной и полихимиотерапии (в 10%);
- курение;
- операции по пересадке органов (75% случаев);
- гормональные сбои во время полового созревания.
Саркома у детей
Саркома у подростков и детей стремительно растет и часто дает рецидивы, из-за того, что в этом возрасте активно растет мышечная и соединительная ткани. Это заболевание находится на 2 месте после рака среди онкообразований, диагностируемых у ребенка, и которые приводят к смерти.
Список литературы

АЛТ – Аланинаминотрансфераза
АСТ – Аспартатаминотрансфераза
б/х – биохимический анализ крови
в/в кап. – внутривенно капельно
в/в стр. – внутривенно струйно
ВОЗ – всемирная организация здравоохранения
ВССЮ – внескелетная саркома Юинга
Гр – грей
ДН – динамическое наблюдение
ЖКТ – желудочно-кишечный тракт
ЖНВЛП – жизненно необходимые и важнейшие лекарственные препараты
КСЮ – костная саркома Юинга
л. – литр
ЛДГ– лактатдегидрогеназа
ЛПУ – лечебно-профилактическое учреждение
ЛТ – лучевая терапия
мг – миллиграмм
мг/м2 – миллиграмм на метр квадратный

МКБ 10 – международная классификация болезней (10-й пересмотр)
мл – миллилитр
МРТ – магнитно-резонансная томография
МТС – метастаз
НПВС – нестероидные противовоспалительные средства
ОАК – общий анализ крови
ОАМ – общий анализ мочи

ОССЮ – опухоль семейства саркомы Юинга
ПЗ – прогрессия заболевания
ПНЭО – периферическая примитивная нейроэктодермальная опухоль кости
ПХТ – полихимиотерапия
ПЭ – полный эффект
ПЭТ -КТ – позитронно-эмиссионная томография
РД – разовая доза
РД – разовая доза
РИД – радиоизотопное исследование
РКТ- рентгеновская компьютерная томография
РФ – Российская Федерация
СД – суммарная доза
СОД – суммарная очаговая доза
СТ – симптоматическая терапия

СЮ – саркома Юинга
УЗИ – ультразвуковое исследование
ЧЭ – частичный эффект
ЩФ – щелочная фосфатаза
ЭКГ – электрокардиограмма
ET – Этопозид (Etoposide), Топотекан (Topotecan)
GEM/TAX – Гемцитабин (GEmcitabinum), Доцетаксел (Docetaxelum)
hr – гипер (hyper)
IE – Ифосфамид (Ifosfamide), Этопозид (Etoposide)
TC – Топотекан (Topotecan), Циклофосфан (Cyclophosphamide)
TEM/IR – Темолозомид (Temozolomidum), Иринотекан (Irinotecanum)
TNM – классификации злокачественных новообразований (Tumor, Nodus, Metastasis)
VAC – Винкристин (Vincristine), Адриамицин (Adriamycin), Циклофосфан (Cyclophosphamide).
VCT – Винкристин (Vincristine), Циклофосфан (Cyclophosphamide), Топотекан (Topotecan)
Лечение саркомы Юинга
Начинающую стадию недуга определить трудно, поскольку симптоматика имеет нечеткую смазанную форму. Ощущаются незначительные и непонятные боли в зоне пораженной кости. По мере прогрессирования недуга в патологический процесс вовлекаются соседние ткани, болевые ощущения становятся интенсивнее. Кости становятся пастозными, утолщаются. Опухоль быстро разрастается, заполняет канал костного мозга и возникают метастазы в мышцах, легких, головном мозге.
В зависимости от интенсивности проявления недуга различают пять стадии:
- Стадия IA. Проявляется естественным ограничением очага, который препятствует разрастанию опухоли. Метастазов нет.
- Стадия IB. Опухоль уже не ограничивается внутренним барьером, но метастазы еще отсутствуют.
- Стадия IIA. Как и в первой стадии, опухоль ограничена барьером, а метастазы не разрастаются.
- Стадия IIВ. Саркома распространяется за внутренние барьеры, метастазы также отсутствуют.
- Стадия III. Наблюдаются близлежащие и отдаленные метастазы.
Остеосаркома имеет следующие разновидности:
- телеангиэктатическая;
- юкстакортикальная;
- периоссальная;
- интраосальная;
- мультифокальная;
- экстраскелетная;
- мелкоклеточная;
- остеосаркома таза.
Это редкие виды рака кости, каждый из которых имеет собственную симптоматику и происхождение.
Телеангиэктатическая — на снимке имеет сходство с аневризмальной костной кистой и гигантоклеточной опухолью. Течение заболевания ничем не отличается от классических вариантов остеосаркомы.
Юкстакортикальная — развивается из коркового слоя кости, а опухолевая ткань окружает кости со всех сторон, но обычно не проникает костномозговой канал. Этот вид остеосаркомы имеет низкий порог злокачественности, протекает медленно и практически не дает метастазов. Однако лечение необходимо проводить своевременно, поскольку эта опухоль способна прогрессировать, и меняет степень злокачественности на более высокую.
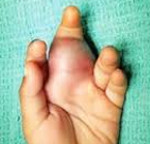
Периоссальная — локализуется на поверхности кости, имеет мягкую структуру, также не проникает в костномозговой канал.
Интраосальная опухоль обладает низкой степенью злокачественности и расценивается как доброкачественная опухоль. Однако при отсутствии адекватного лечения они также склоны к рецидиву в более злокачественный вариант.
Мультифокальная — характеризуется множественными очагами в костях, которые похожи друг на друга. До сих пор не известно, возникают ли они все сразу или же происходит быстрое метастазирование одного очага. Прогноз неблагоприятный.
Экстраскелетная — редкая опухоль, которая проявляется поражением других областей:
- гортани;
- пищевода;
- почек;
- печени;
- кишечника;
- сердца;
- мочевого пузыря.
Прогноз заболевания крайне неблагоприятный. Опухоль очень агрессивная и практически не поддается химиотерапии.
Мелкоклеточная опухоль обладает высокой степенью злокачественности. По своей морфологии отличается от всех остальных видов. Чаще всего поражает бедренную кость.
Остеосаркома таза характеризуется крайне неблагоприятным прогнозом. Опухоль быстро прогрессирует и широко распространяется в соседние ткани, поскольку из-за своего анатомического строения не встречает на своем пути фасциальных барьеров.
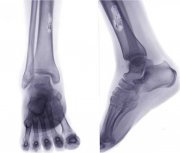
Также разделяют следующие типы остеосаркомы:
- остеолитическую;
- склеротическую;
- смешанную.
Остеолитическая саркома проявляется присутствием одиночного очага, который имеет нечеткие границы. Разрушения кости быстро прогрессирует, увеличиваясь в длину и ширину. Происходит поражение мягких тканей, затем метастазы проникают в другие органы.
Остеопластическая форма приводит к быстрому росту новообразования, что ведет к разрушению костной ткани. Опухоль быстро заполняет пустоты в губчатом веществе, образуя игольчатые разрастания.
Смешанная форма подразумевает комбинацию симптомов двух выше перечисленных видов саркомы.
Данный вид рака кости является одним из распространенных злокачественных заболеваний опорно — двигательного аппарата. Опухоль очень агрессивна, быстро растет и склонна к раннему метастазированию. Этот вид рака кости появляется у детей и подростков от 10 до 20 лет. Болезнь в большей степени поражает мужчин, нежели женщин.
Остеогенная саркома называется первичной, поскольку происходит непосредственно из костной ткани. Она также локализуется преимущественно в метафизе цилиндрические или трехгранные костей нижних и верхних конечностях:
- в бедренной;
- плечевой;
- малоберцовой;
- лучевой;
- локтевой кости.
В редких случаях остеосаркома развивается в костях черепа, таза и стопах. По мере роста опухоль у детей распространяется на мышечную и фиброзную ткань, а также проникает в мозговой канал.
Развивается недуг у детей по причине:
- воздействия ионизирующего излучения;
- канцерогенов и токсических веществ;
- генетической предрасположенности;
- врожденных аномалий и патологий костной ткани (болезнь Педжета, фиброзная дисплазия);
- в результате воспалительных заболеваний.
Вышеназванные факторы запускают механизмы опухолевого роста, которые начинаются с нарушения внутриклеточных процессов: деления и роста клеток. Они провоцируют появление атипичных клеток, которые начинают бесконтрольно размножаться. Так возникают опухоли у детей и подростков. Распространенность недуга связана с бурным ростом скелета. В этой ситуации чрезмерные физические нагрузки могут сыграть отрицательную роль.
Одно время считалось, что травма может инициировать развитие раковой опухоли. Поскольку иногда остеосаркома возникает в результате переломов или ушибов. Однако специалисты пришли к выводу, что травма является катализатором появления боли, но не является причиной саркомы. Именно патологические изменения в структуре костей приводят к переломам.
Дебютирует недуг бурно, остро и стремительно. Наблюдается боль, особенно в ночное время, резкое похудение, постоянная усталость и сонливость. На поздних стадиях наблюдается повышение температуры до 38 — 39ᵒС. Однако эти симптомы не всегда свидетельствуют о наличии этого грозного заболевания. В детском возрасте намного чаще наблюдаются доброкачественные заболевания костной системы.
Лечение рака кости у детей проводят комплексно. Оно подразумевает:
- предварительную химиотерапию;
- хирургическое лечение;
- послеоперационную терапию.
В основном лечение рака кости у ребенка предполагает химиотерапию и хирургическое лечение. Лучевую терапию применяют только в случае, когда нет возможности провести радикальное удаление злокачественной опухоли.
Эта разновидность рака кости встречается преимущественно у детей и располагается чаще всего в костях, реже может развиться в мягких тканях: соединительной, мышечной, жировой и тканях периферических нервов. Саркома Юинга крайне агрессивна и дает метастазы так быстро, что без адекватного и быстрого лечения эта болезнь смертельна.
Эта форма рака кости встречается достаточно редко. Она поражает преимущественно детей и подростков, однако встречается и у очень пожилых людей. Мальчики и мужчины болеют значительно чаще девочек. Больше половины всех заболевших это дети и подростки возрастного интервала от 10 до 20 лет.
Саркома Юинга может поразить любую кость. Чаще всего опухоль выявляется в тазовых костях, также может появиться в длинных трубчатых костях бедра, голени и ребер. Опухоль может распространиться и внутри кости, и в мягких тканях вокруг кости. Иногда она может сразу вырасти в мягких тканях вокруг кости, а в самой кости ее может не быть.
Чаще всего встречается остеогенная саркома бедренной и большой берцовой кости — в области коленного сустава. Типичный симптом заболевания — упорные боли в суставе, кости. Иногда они постоянные, а иногда то стихают, то нарастают. Болевые ощущения могут усиливаться по ночам, во время физической активности (при ходьбе, беге, занятиях спортом). Если поражена нога, человек начинает хромать.
В области опухоли можно обнаружить отек или нащупать «шишку», уплотнение. Несмотря на то что опухолевая ткань ослабляет кость, переломы случаются не так часто.
Дети, особенно маленькие, физически активны, они часто падают, ударяются, поэтому у них первые симптомы остеосаркомы легко спутать с травмой. У взрослого человека, особенно если он не занимается спортом и тяжелым физическим трудом, подобные проявления сразу должны насторожить и стать причиной для визита к врачу.
Остеосаркома челюсти чаще всего встречается в возрасте 20–40 лет, то есть в среднем на 10 лет позже, чем «обычные» остеосаркомы. Проявляется в виде болей, припухлости, деформации зубов. Иногда опухоль затрудняет глотание, дыхание.
Симптоматика саркомы зависит от ее места расположения в жизненно важных органах. Оказывает влияние на характер симптомов особенности первичных клеток и самой образовавшейся опухоли.
Раньше всего проявляются болевые ощущения в суставах и костях (чаще ночью), которую не могут купировать анальгетики.
Печени
Диагностируется редко, проявляется симптоматикой в зоне правого подреберья. Больные теряют в весе, кожа желтеет, вечерами может наблюдаться гипертермия;
Желудка
Начало заболевания всегда бессимптомно и обычно заболевание выявляется случайно. Появляются диспепсические нарушения вроде тошноты, тяжести, метеоризма и вздутия. Появляются признаки истощения, больной чувствует утомленность, депрессию, раздражительность;
Кишечника
Сопровождаются болями в области живота, тошнотой, отсутствием аппетита, нарушения в работе кишечника, выделениями кровянисто-слизистой структуры из прямой кишки, дефекационными позывами, истощением организма;
Имеет ярко выраженную гематурию, болезненность в месте расположения опухоли, при пальпации она прощупывается, наблюдается кровь в моче;
Саркома может вырасти до больших величин, сжимая рядом расположенные ткани, разрушая корешки нервных окончаний, элементы позвоночника, это дополняется интенсивной болью в соответствующих местах. Иногда такого типа саркома может стать причиной паралича или пареза.
Селезенки
На ранних этапах может никак не проявляться, но с ростом образования, а следующим распадом, происходит интоксикации (субфебрильная температура, анемия и прогрессирующая слабость. Также могут возникать: постоянное ощущение жажды, отсутствие аппетита, апатия, рвотный синдром, учащенные позывы к мочеиспусканию;
Первым, самым ранним признаком заболевания становится боль в области поражения. Вначале она слабая или умеренная, самопроизвольно ослабевает или исчезает, а затем появляется снова. В отличие от болей при воспалительных процессах такая боль не ослабевает в покое, по ночам или при фиксации конечности. Напротив, для саркомы Юинга характерно усиление болей в ночное время.
По мере прогрессирования боли становятся более интенсивными, лишают сна и ограничивают повседневную активность. В близлежащем суставе развивается болевая контрактура. Пальпация области поражения болезненна. Температура кожи над ней повышена. Отмечается пастозность мягких тканей, местная гиперемия и расширение подкожных вен. Опухоль быстро увеличивается и (обычно спустя несколько месяцев после возникновения первых симптомов) становится настолько крупной, что ее можно прощупать. На поздних стадиях в области новообразования нередко возникает патологический перелом.
Местные клинические признаки сочетаются с нарастающими симптомами общей опухолевой интоксикации. Больные предъявляют жалобы на слабость и потерю аппетита. Отмечается снижение веса вплоть до истощения. Температура тела повышена до субфебрильных или даже фебрильных цифр. Определяется регионарный лимфаденит. По анализам крови выявляется анемия.
Некоторые симптомы зависят от локализации новообразования. Так, при возникновении саркомы Юинга на костях нижних конечностей появляется хромота. При поражении позвонков возможно развитие компрессионно-ишемической миелопатии с нарушением функции тазовых органов и явлениями параплегии. При новообразованиях в области костей грудной клетки может возникнуть дыхательная недостаточность, плевральный выпот и кровохарканье.
Поскольку данная опухоль относится к категории высокоагрессивных неоплазий, рано дающих метастазы, ее лечение должно включать в себя воздействие на весь организм, а не только на первичный очаг, даже в тех случаях, когда метастазы не были обнаружены. Дело в том, что существует очень высокая вероятность раннего появления микрометастазов, которые на момент постановки диагноза невозможно выявить при помощи существующих методов. Лечение саркомы Юинга комбинированное, включает в себя как консервативную терапию, так и хирургические вмешательства и состоит из следующих компонентов:
- Пред- и послеоперационная химиотерапия, как правило – с использованием нескольких препаратов (доксорубицин, винкристин, циклофосфан, ифосфамид, этопозид и актиномицин в различных комбинациях). После курса лечения оценивается ответ опухоли на терапию. Хорошим результатом считается наличие не более 5% живых клеток опухоли.
- Лучевая терапия с использованием высоких доз. Проводится на первичный очаг, а, при наличии метастазов в легочную ткань – и на легкие.
- Хирургическая операция. Если это возможно, опухоль удаляют радикально, вместе с мягкотканым компонентом. При этом удаленный участок кости заменяют эндопротезом. Но даже если в силу места расположения и размера новообразования удалить его полностью не представляется возможным, оперативное лечение (частичная резекция) позволяет улучшить контроль над опухолью и повысить шансы на благополучный исход.
В прошлом при саркоме Юинга обычно проводились калечащие операции – ампутации и экзартикуляции. Современные техники позволяют выполнять органосохраняющие оперативные вмешательства не только на мелких (малоберцовой, лучевой, локтевой, лопатке, ключице и ребрах), но и на крупных костях (плечевой, бедренной и даже костях таза). При метастазировании в костный мозг и кости назначается интенсивная терапия, включающая в себя тотальное облучение всего тела, химиотерапию с использованием мегадоз препаратов и трансплантацию периферических стволовых клеток или костного мозга.
Термины и определения
Анализ выживаемости (от анг. Survival analysis) — это класс статистических моделей, позволяющих оценить вероятность наступления события.
Инструментальная диагностика – диагностика с использованием для обследования больного различных приборов, аппаратов и инструментов.
Лабораторная диагностика — совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Медицинское вмешательство – выполняемые медицинским работником и иным работником, имеющим право на осуществление медицинской деятельности, по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, диагностическую, лечебную, реабилитационную или исследовательскую направленность виды медицинских обследований и (или) медицинских манипуляций, а также искусственное прерывание беременности.
Медицинский работник – физическое лицо, которое имеет медицинское или иное образование, работает в медицинской организации и в трудовые (должностные) обязанности которого входит осуществление медицинской деятельности, либо физическое лицо, которое является индивидуальным предпринимателем, непосредственно осуществляющим медицинскую деятельность.
Полный эффект (ПЭ) – полная регрессия мягкотканного компонента опухоли, отсутствие или исчезновение отдаленных метастазов, положительная динамика в виде ис-чезновения периостальной реакции, уменьшение остеолитических очагов по дан-ным рентгенологического, КТ и МРТ исследований.
Прогрессия заболевания (ПЗ) – прогрессия более 25% от первоначального объема поражения или появление новых метастазов.
Рабочая группа – двое или более людей одинаковых или различных профессий, работающих совместно и согласованно в целях создания клинических рекомендаций, и несущих общую ответственность за результаты данной работы.
Синдром – совокупность симптомов с общими этиологией и патогенезом.
Хирургическое вмешательство – инвазивная процедура, может использоваться в целях диагностики и/или как метод лечения заболеваний.
Хирургическое лечение — метод лечения заболеваний путём разъединения и соединения тканей в ходе хирургической операции.
Частичный эффект (ЧЭ) – редукция более 50% опухолевой массы по сравнению с первоначально диагностированным объемом. Стабилизация заболевания (СЗ): сокращение менее 50% или прогрессия менее 25% от первоначального объема опухолевого поражения.
Саркома Юинга (СЮ) – это злокачественная опухоль костной ткани, состоящая из широких полей небольших округлых клеток без межуточного вещества (ВОЗ 2002 г.) [1,6]. В 1990-х годах в мировой литературе был принят термин «опухоли семейства саркомы Юинга» (ОССЮ). Данная группа включает [2]:
- костную саркому Юинга (КСЮ),
- внескелетную саркому Юинга (ВССЮ),
- периферическую примитивную нейроэктодермальную опухоль кости (ПНЭО)
- злокачественную мелкоклеточную опухоль торакопульмональной зоны (опухоль Аскина).
ИНФОРМАЦИЯ О ПРЕПАРАТАХ
Адриамицин, эпирубицин и идарубицин, будучи антрациклинами, имеют сходный механизм действия и спектр токсичности. Для оценки риска поздних токсических эффектов следует рассчитывать кумулятивную дозу всех типов антрациклинов. Актиномицин D (AMD):Механизм действия: Ингибирование синтеза ДНК. Побочные эффекты:

Связанные с токсичностью побочные эффекты, кроме тошноты и рвоты, обычно возникают через 2–4 дня после окончания химиотерапии. Обычные побочные эффекты – раздражение желудочно-кишечного тракта (потеря аппетита, тошнота, рвота, гастроэнтерит, понос, боли в животе, язвенный стоматит, анорексия, черный стул/кровь в стуле), гепатотоксичность (веноокклюзивная болезнь, особенно у маленьких детей;
асцит, гепатомегалия, гепатит, изменения уровней печеночных ферментов, изменения кроветворения), подавление функции костного мозга, алопеция, экзантема и дерматит (кожная сыпь, угри, гиперпигментация, отсроченные реакции в ранее облученных областях [radiation recall reaction]). Могут наблюдаться утомляемость, слабость, подавленность, лихорадка/озноб, мышечные боли, проктит, нарушение почечной функции, гипокальциемия, раздражение интимы (при внутривенном введении).
Только парентеральное применение. Разовая доза не должна превышать 2.0 мг. Препарат может вводиться через периферическую в/в канюлю или через центральный катетер с принятием необходимых мер во избежание экстравазации. Доксорубицин (ADR): Механизм действия: Ингибирование синтеза ДНК (интеркаляция в ДНК и ингибирование ДНК-топоизомеразы II).
Побочные эффекты: Миелосупрессия, острая и поздняя кардиотоксичность (преходящая аритмия, застойная сердечная недостаточность, дозозависимая кардиомиопатия), раздражение желудочно-кишечного тракта (тошнота, рвота, потеря аппетита, диарея, стоматит, изъязвление), аллергические реакции с кожной сыпью, лихорадка и озноб, алопеция, дерматит (покраснение лица, гиперпигментация, изменения ногтей), отсроченные реакции в ранее облученных областях (radiation recall), красный цвет мочи в течение 1–2 дней, бесплодие.
Было показано, что ADR обладает мутагенными и канцерогенными свойствами. Эктстравазация может вызвать локальный некроз.Введение: Только парентеральное применение. Более продолжительная инфузия ({amp}gt;12 ч), как представляется, не имеет кардиопротекторного эффекта и может повышать риск мукозита, особенно если ADR вводится совместно с актиномицином D (см.
информацию о препаратах). Препарат может вводиться через периферическую в/в канюлю или через центральный катетер с принятием необходимых мер во избежание экстравазации. Важен тщательный мониторниг функции сердца. С осторожностью при параллельном применении других кардиотоксических препаратов или облучении грудной клетки.
Карбоплатин (CARBO): Механизм действия: Алкилирующий, цитотоксический препарат.Побочные эффекты: Миелосупрессия (тромбоцитопения, реже лейкопения, нейтропения и анемия). Гиперчувствительность: анафилаксия и анафилактоидная реакция с бронхоспазмом и падением артериального давления, зудом, кожной сыпью, лихорадкой, ознобом и отеком.
Тошнота и рвота, болезненное раздражение желудочно-кишечного тракта, желудочные боли, спазмы, потеря аппетита, снижение веса, понос, запор, анорексия, инфекции и/или кровотечения, дрожь, нарушения вкусовых ощущений, мукозит. Нейротоксичность: периферическая сенсорная нейропатия, астения. Известны случаи воспаления зрительного нерва и ухудшения зрения, слепоты.
Геморрагический цистит (микро- и макрогематурия у 10% пациентов, получающих низкодозный циклофосфамид, и у 40% получающих высокодозный CYC), задержка жидкости с гипонатриемией, гиперурикемией (в периоды острого лизиса клеток), синдром неадекватной секреции антидиуретического гормона. Миелосупрессия.
Иммуносупрессия. Кардиотоксичность (геморрагический некроз), особенно при использовании высокодозного CYC. Редко анафилактические реакции. Химический флебит в месте укола, возможные отсроченные реакции в ранее облученных областях (radiation recall). Редко – острый интерстициальный пневмонит или хронический легочный фиброз.
Аменорея, нарушения функции яичников, азооспермия, бесплодие. Ощущение заложенности носа или неприятные ощущения в лице во время введения препарата. Вторичные злокачественные заболевания. Введение: Пероральное или парентеральное введение. Необходимо перед введением исключить почечную дисфункцию, непроходимость мочевых путей, инфекции и электролитные нарушения.
тошнота и рвота, стоматит, понос; алопеция, крапивница, химический флебит в месте укола. Отсроченные реакции в ранее облученных областях (radiation recall). В случае одновременного введения эпирубицина и цитостатиков, взаимодействующих с ДНК, в некоторых случаях вторичные злокачественные опухоли, даже спустя недолгое время.

Иногда лихорадка, озноб, гепатотоксичность. Красное окрашивание мочи в течение 1–2 дней.Введение: Только внутривенное применение. Обратите внимание на кумулятивный риск кардиотоксичности при введении антрациклинов. Необходимо скорректировать дозировки при сердечно-сосудистых заболеваниях и при гепатотоксичности.
Этопозид (ETO):Механизм действия: Ингибирование топоизомеразы II. Синоним: VP-16.Побочные эффекты: Дозозависимая миелосупрессия с лейкопенией, нейропенией, тромбоцитопенией, анемией, инфекциями (пневмония, сепсис). Тошнота и рвота, мукозит, стоматит, боли в животе, потеря аппетита, запор, изменения вкусовых ощущений.
Слабость, утомляемость, головные боли, озноб, лихорадка, обратимая алопеция. Химический флебит в месте укола. Кровотечения, в том числе петехиальные; кровохарканье, боли в груди, преходящая одышка. Легочная эмболия. Нейротоксичность (редко): мышечные боли, нарушения функции центральной нервной системы (раздражение, сонливость, гиперкинезия, акинезия), периферическая нейропатия, обратимая потеря центрального зрения.
Тяжелые реакции гиперчувствительности: озноб, лихорадка, тахикардия, бронхоспазм, одышка, артериальная гипотензия, зуд, кожная сыпь. Анафилактоидная реакция при в/в введении и преходящее снижение артериального давления при быстром в/в введении, апноэ с самопроизвольным восстановлением дыхания после прекращения инфузии, артериальная гипертензия, покраснение кожи, кожные реакции (экзема, крапивницы, пигментация, зуд).
В отдельных случаях – серьезное повышение уровня печеночных ферментов и функциональных печеночных проб, острый лейкоз, инфаркт миокарда и аритмия, синдром Стивенса-Джонсона (без доказательств причинной связи с введением ETO). Введение: Пероральное или парентеральное введение. Обратите внимание на потерю эффективности в случае параллельного применения этопозида фосфата с ингибиторами фосфатазы.
Перекрестная резистентность с антрациклинами. Корректировка дозы при печеночной недостаточности и нейротоксичности.Идарубицин (IDA): Механизм действия: Интеркаляция в ДНК и ингибирование ДНК-топоизомеразы II, противоопухолевый антибиотик. Побочные эффекты: Кардиотоксичность, аритмии (редко, преходящие), застойная сердечная недостаточность (дозолимитирующее осложнение).
Миелосупрессия (дозолимитирующее осложнение), желудочно-кишечные симптомы: тошнота и рвота, стоматит, понос, нейтропенический энтероколит с перфорацией. Химический флебит в месте инъекции, преходящее повышение функциональных печеночных проб, гиперчувствительность (сыпь, лихорадка, озноб), алопеция, покраснение лица при быстром введении, отсроченные реакции в ранее облученных областях (radiaton recall) – редко.
Механизм действия: Алкилирующий препарат.Побочные эффекты: Геморрагический цистит (микро- и макрогематурия), нефротоксичность (тубулопатия с глюкозурией, аминоацидурией, потерями фосфата и кальция, полный спектр тубулопатий от субклинических изменений до выраженного синдрома Фанкони). Нейротоксичность с преходящей сонливостью, дезориентацией, депрессивным психозом, галлюцинациями, ментальными расстройствами, редко с судорожными приступами в 10–20% случаев.
Подавление функции костного мозга, иммуносупрессия, раздражение желудочно-кишечного тракта (тошнота, рвота, понос, стоматит), лихорадка и озноб, алопеция, бесплодие, нарушения овуляции, аллергические реакции. Редко – печеночная дисфункция, легочный фиброз, пневмонит и кардиотоксичность. IFO обладает потенциально мутагенными, тератогенными и канцерогенными свойствами;
Антиметаболит. Конкурентное ингибирование дигидрофолатредуктазы ведет к блокированию синтеза тетрагидрофолата.Побочные эффекты: Желудочно-кишечные симптомы: тошнота, рвота, геморрагический энтерит, перфорация кишечника, понос, анорексия. Миелосупрессия, иммуносупрессия, мегалобластоз. Повышенные функциональные печеночные пробы (временно), печеночный фиброз, цирроз.
Анафилактические реакции (редко), лихорадка и озноб (редко). Конъюнктивит. Отсроченные реакции в ранее облученных областях (radiation recall), алопеция, депигментация, гиперпигментация, фоточувствительность, эритематозная сыпь. Химический менингит (редко), острая энцефалопатия (в высоких дозах), лейкоэнцефалопатия (редко).
Отек легких, плевральные боли в груди, интерстициальный пневмонит, токсическая нефропатия (при высоких дозировках). Выкидыши, пороки внутриутробного развития. Введение: Пероральное или парентеральное введение. С осторожностью при печеночной дисфункции. Тиотепа:Механизм действия: Алкилирующий препарат.
Побочные эффекты: тошнота, рвота, анорексия, миелосупрессия, мукозит, эзофагит, гонадная дисфункция, боль в месте введения, головокружения, головные боли, крапивница, кожная сыпь. Фебрильные реакции (редко). Анафилактические реакции (редко). Введение: Внутривенное или интратекальное. Необходимо учитывать кумулятивную токсичность и избегать параллельного облучения.

Пероральный прием при поддерживающей терапии в амбулаторном режиме. Исключить прием трофосфамида при нейтропении и почечной дисфункции. Винбластин (VBL):Механизм действия: Ингибитор митоза, блокирует полимеризацию микротрубочек.Побочные эффекты: Нейропатии с поражением вегетативной нервной системы (запор, боли в животе, задержка мочи, паралитический илеус) и черепно-мозговых нервов (парез или паралич голосовых связок, дисфункция глазодвигательного нерва, двусторонние параличи лицевых нервов, челюстные боли), нейротоксичность (онемение, парестезии, депрессии, потеря глубоких сухожильных рефлексов, головные боли, ощущения дискомфорта, головокружения, судороги или психозы).
Некроз тканей при экстравазации, боли при инъекции, химический флебит. Гиперурикемия в периоды активного лизиса клеток, в редких случаях синдром нарушенной секреции антидиуретического гормона. Миелосупрессия, иммуносупрессия. Анафилактические реакции (редко). Желудочно-кишечные симптомы: небольшая тошнота и рвота, стоматит, запоры, боли в животе, паралитический илеус.
Боли в мышцах и в опухоли. Бесплодие. Синдром Рейно. Алопеция (часто), фоточувствительность (редко). Экстравазация может привести к тяжелому локальному и региональному изъязвлению.Введение: Только внутривенное введение. Смертелен при интратекальном введении. Необходима корректировка дозы при неврологических побочных эффектах.
Препарат должен вводиться через периферическую в/в канюлю или центральный катетер с принятием должных мер во избежание экстравазации. Винкристин (VCR):Механизм действия: Ингибитор митоза; блокирует полимеризацию микротрубочек.Побочные эффекты: Нейропатии периферических и черепно-мозговых нервов, включая запор и/или паралитический илеус, птоз, паралич голосовых связок, челюстные боли, арефлексию, парестезии, мышечную слабость, атаксию (в норме обратимую);
центральная нейротоксичность (включая галлюцинации, судороги, синдром нарушенной секреции антидиуретического гормона, атрофию зрительного нерва, двоение в глазах, временную слепоту), боли в суставах и мышцах, минимальное подавление функции костного мозга, утомляемость, головные боли, головокружения, депрессия, алопеция, раздражение желудочно-кишечного тракта (небольшая тошнота и рвота, потеря аппетита, спазмы, понос, стоматит), атония мочевого пузыря, нарывы.
Потенциально мутагенное и канцерогенное действие. Экстравазация может привести к тяжелому локальному и региональному изъязвлению.Введение: Только внутривенное применение. Смертельно при интратекальном введении. Разовая доза не должна превышать 2.0 мг. Корректировка доз при печеночной недостаточности или неврологических побочных эффектах. Препарат должен вводиться через периферическую в/в канюлю или центральный катетер с принятием должных мер во избежание экстравазации.
Остеосаркома бедренной кости
- Биопсия кости игольная — 18 200 руб.
- Краевая резекция, экскохлеация бедренной кости с ксенопластикой — 230 100 руб.
- Краевая резекция, экскохлеация плоской кости с ксенопластикой — 230 100 руб.
- Открытая биопсия костного опухолевого очага — 97 000 руб.
- Радиочастотная аблация новообразований костей и мягких тканей — 149 000 руб.
- Экскохлеация трубчатой кости с замещением дефекта биокомпозитным материалом — 139 900 руб.
Наиболее благоприятен прогноз в случаях, когда опухоль локализованная — то есть не успела распространиться по организму и может быть полностью удалена во время операции. Пятилетняя выживаемость составляет 60–80%, а если опухоль чувствительна к современным таргетным препаратам — до 90%.
Если есть метастазы остеосаркомы, прогноз сильно ухудшается. Пятилетняя выживаемость падает до 15–30%. Но она может быть выше, в пределах 40%, если:
- рак успел распространиться только в легкие;
- все метастазы можно обнаружить и удалить.

Метастазы остеосаркомы чаще всего обнаруживают в легких, реже в костях, головном мозге и других местах.
В настоящее время точные причины этого заболевания до конца неизвестны. Однако можно выделить несколько факторов, которые способны спровоцировать развитие патологии. К ним можно отнести контакты:
- с канцерогенами;
- ионизирующим излучением;
- химическими веществами;
- вирусами.
Часто остеосаркома развивается в результате травмы. Однако это не является причиной, а катализатором для возникновения опухоли.
Основной причиной саркомы бедренной кости является быстрый рост скелета во время пубертатного периода. Другой причиной являются генетические аномалии, в частности мутация определенных генов.
На начальной стадии развития заболевание никак не проявляется. Затем при разрастании опухоли появляются болевые ощущения, нарушаются функции конечностей, появляется припухлость. По мере прогрессирования патологический процесс поражает все новые ткани и суставы, а кости прорастают в костный мозг. Злокачественные клетки распространяются с кровью по всему организму, образуя метастазы в внутренних органах.
Лечение недуга включает в себя:
- предоперационную терапию;
- хирургическое лечение;
- послеоперационная терапия.

Предоперационная терапия проводится с целью уменьшения опухоли. Для этого используют препараты из группы цитостатиков.
Хирургическое лечение предполагает радикальную ампутацию пораженной конечности. Однако в настоящее время рак бедренной кости лечится более щадящим способом. Орган сохраняют, удаляя патологическое образование, а взамен вставляют имплантат.
Послеоперационную химиотерапию проводят для уничтожения оставшихся злокачественных клеток, а также для удаления очагов метастазирования. К сожалению, даже такое лечение не всегда дает полное избавление от рака кости. Остеосаркома может рецидивировать через 2- 3 года и симптомы появляются снова.
1.2 Этиология и патогенез
Новообразование описано и выделено в самостоятельную нозологическую форму Джеймсом Юингом [3] в 1921 г. Поскольку изначально автор предполагал, что опухоль развивается из клеток периваскулярного эндотелия, то назвал ее «диффузной эндотелиомой кости» и позже предложил обозначать как «эндотелиальную миелому кости».
Близкое родство этих новообразований подтверждается характерной генетической особенностью: наличием единой хромосомной транслокации t(11;22) (q12; 24), повреждающей ген EWS, или ее варианта t(21;22). Однако, по данным ряда авторов, несмотря на аналогичное происхождение опухолей и одинаковый подход к лечению, наблюдается различная степень их дифференцировки и различный прогноз. Так, для ПНЭО характерны более выраженная нейроэктодермальная дифференцировка и более агрессивное течение.
У 25% пациентов опухоль локализуется в костях таза, в то время как у 50% опухоль локализуется на конечностях. Кроме того, достаточно часто поражаются ребра и позвоночник. Саркома Юинга может поражать любые кости и (реже у пациентов детского возраста) возникает исключительно в мягких тканях [1,2].
Прогноз саркомы
Прогноз зависит от некоторых факторов:
- размер и местоположение новообразования;
- стадия заболевания (локализация опухоли, наличие метастазов в других органах);
- возраст и общее состояние здоровья пациента.
Послеоперационный прогноз зависит от эффективности предоперационной химиотерапии и результата операции. Наиболее благоприятный прогноз — существенное уменьшение метастазов после химиотерапии, а также при полном удалении опухоли.

В прошлые времена остеосаркома позиционировалась как серьезный злокачественный недуг с весьма неблагоприятным исходом (даже при удалении конечности выживаемость составляла не более 5 — 10%). В настоящее время, благодаря новым методам лечения и эффективным органосохраняющим хирургическим вмешательствам, шансы на благополучный прогноз существенно увеличились даже при наличии метастазов в других органах.
Что касается профилактики, то в настоящее время нет эффективных профилактических мер против этого недуга. Специалисты советуют своевременно лечить травмы и повреждения суставов и костей. Людям с наследственной предрасположенностью к недугу рекомендуется регулярно наблюдаться у врача для выявления первых признаков перерождения костной ткани.
Прогнозы для онкобольных выстраивают на основе особого показателя — пятилетней выживаемости. Он обозначает процент пациентов, которые остались живы в течение пяти лет с момента установления диагноза. Конечно, многие живут и дольше. Пять лет — условный рубеж, после которого можно с достаточно высокой вероятностью предполагать, что человек выздоровел.
Своевременное комбинированное лечение обеспечивает 70% общую выживаемость пациентов с локализованной саркомой Юинга. При наличии метастазов в кости и костный мозг прогноз существенно ухудшается, однако сочетание высокодозной химиотерапии, тотальной лучевой терапии и трансплантации костного мозга дает возможность повысить выживаемость больных с метастатической формой заболевания с 10% до 30% и более.
Все пациенты после излечения должны проходить регулярное обследование для раннего выявления рецидивов и контроля над побочными эффектами. Следует учитывать, что ряд побочных эффектов может возникать не только при прохождении курса лечения, но и спустя длительное время после его окончания. К числу таких эффектов относится мужское и женское бесплодие, кардиомиопатия, нарушение роста костей и увеличение вероятности развития вторичных злокачественных новообразований. Однако многие пациенты, прошедшие лечение по поводу саркомы Юинга могут жить полноценной жизнью. Профилактика не разработана.
Прогнозы при заболевании зависят от стадии опухолевого процесса, его формы, локализации, наличия метастаз. Если опухоль диагностирована на последней стадии, то больному остается жить совсем немного.
При саркоме мягких тканей и конечностей 5-летняя выживаемость составляет около 75%, при онкопроцессе на теле — до 60%.
Чем ниже дифференцировка опухолевых клеток, тем тяжелее пациента вылечить. Это зависит от того, что несозревшая клетка обычно дает метастазы. Но современные лекарственные препараты позволяют сильно снизить риск смертельного исхода. В 90 % случаев своевременная и адекватная терапия сильно увеличивает продолжительность жизни или полностью излечивает пациента.
1.4 Кодирование по МКБ 10
| C40 | Злокачественное новообразование костей и суставных хрящей конечностей |
| C40.0 | ЗНО лопатки и длинных костей верхней конечности |
| C40.1 | ЗНО коротких костей верхней конечности |
| C40.2 | ЗНО длинных костей нижней конечности |
| C40.3 | ЗНО коротких костей нижней конечности |
| C40.8 | Поражения костей и суставных хрящей конечностей, не перечисленные выше |
| C41 | Злокачественное новообразование костей и суставных хрящей других и неуточненных локализаций |
| C41.0 | ЗНО костей черепа и лица |
| C41.1 | ЗНО нижней челюсти |
| C41.2 | ЗНО позвоночного столба |
| C41.3 | ЗНО ребер, грудины и ключицы |
| C41.4 | ЗНО костей таза, крестца и копчика |
| C41.8 | Поражение костей и суставных хрящей, выходящее за пределы вышеуказанных локализаций |
| C49 | Злокачественное новообразование других типов соединительной и мягких тканей |
| C49.0 | ЗНО соединительной и мягких тканей головы, лица и шеи |
| C49.1 | ЗНО соединительной и мягких тканей верхней конечности |
| C49.2 | ЗНО соединительной и мягких тканей нижней конечности |
| C49.3 | ЗНО соединительной и мягких тканей грудной клетки |
| C49.4 | ЗНО соединительной и мягких тканей живота |
| C49.5 | ЗНО соединительной и мягких тканей таза |
| C49.6 | ЗНО соединительной и мягких тканей туловища неуточненной локализации |
| C49.8 | Поражение соединительной и мягких тканей, выходящее за пределы вышеуказанных локализаций |
| C49.9 | ЗНО соединительной и мягких тканей неуточненной локализации |
Классификация заболевания
По происхождению они делятся на:
- опухоли, которые формируются из твердых тканей;
- опухоли из мягкотканых структур.
По механизму развития разделяют два вида:
- первичная. В этом случае опухоль развивается из тканей того органа, где локализована саркома;
- вторичная. Этот вид содержит клетки, не относящиеся к органу, где расположена опухоль.
По степени злокачественности:
- высокозлокачественные, которым присущи быстрый рост опухолевых клеток и деление, они содержат малое количество стромы и у них хорошо развита система сосудов;
- низкозлокачественные, у которых деление клеток идет с небольшой активностью, они хорошо дифференцируются, содержат мало опухолевых клеток, сосудов мало, а стромы – много.
По степени дифференцировки:
- Gх – нельзя определить дифференцировку клеток;
- G1 – высокодифференцированная саркома;
- G2 – умереннодифференцированная;
- G3 – низкодифференцированная;
- G4 – недифференцированная.
Классификация заболевания по коду Мкб 10 выглядит так:
- С45 — мезотелиома. Она растет из мезотелия, распространяется в перикард, плевру, брюшину;
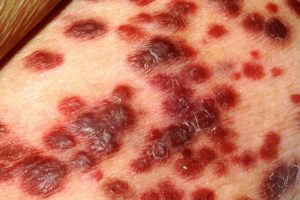
- С46 — саркома Капоши. Поражает кровеносные сосуды, на коже могут появиться красно-бурые пятна. Относится к крайне агрессивным опухолям;
- С47 — опухоль периферической и вегетативной нервной системы. Чаще развивается в нижних конечностях, в области грудной клетки, шеи, бедер, таза;
- С48 — новообразования забрюшинного пространства и самой брюшины;
- С49 — злокачественные новообразования мягкой и соединительной ткани прочих типов.
По месту локализации — обычно саркомы развиваются в зоне:
- кишечника и желудка (опухоли стромальные);
- головы, шеи, в костях;
- женских половых органов (матке) и молочных желез;
- брюшины и забрюшинного пространства;
- мягких тканей туловища и конечностей.
По типу ткани:
- липосаркома, развивающаяся из жировой ткани;
- фибросаркома (дерматосаркома), является фибробластическим (миофибробластическим) образованием;
- фиброгистиоцитарная опухоль мягких тканей — плексиформная и гигантоклеточная;
- лейомиосаркома, образуется из гладкой ткани мышц;
- гломусная опухоль (перицитарная или периваскулярная);
- рабдомиосаркома из мускулатуры скелета;
- миосаркома (из ткани мышц);
- ангиосаркомаи эпителиоидная гемангиоэпителиома, которые считаются сосудистыми новообразованиями мягких тканей, крови и лимфы;
- экстраскелетная остеосаркома, мезенхимальная хондросаркома – опухоли костнохрящевые;
- мезенхимома (эмбриональная опухоль);
- стромальная (злокачественная) опухоль ЖКТ;
- нейрофибросаркома (из клеток нервных оболочек, менингеальная);
- опухоль ствола нерва: периферического, гранулоклеточная, эктомезенхимома, тритон опухоль;
- неясной дифференцировки: светлоклеточная, десмопластическая круглоклеточная, синовиальная, интимальная;
- недифференцированная (неклассифицируемая): веретеноклеточная опухоль, плеоморфная, круглоклеточная, эпителиоидная.
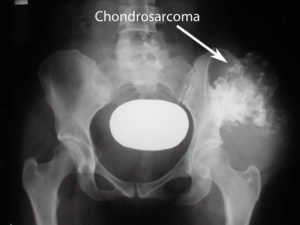
- хрящевой ткани – хондросаркома: центральная, первичная или вторичная, периферическая (периостальная), светлоклеточная, мезенхимальная;
- костной ткани – остеосаркома, Саркома Юинга, хондробластическая, фибробластическая, периостальная и поверхностная высокой степени злокачественности, параостальная, остеобластическая, телеангиэктатическая, мелкоклеточная;
- кроветворной ткани — плазмоцитома (миелома), злокачественная лимфома;
- гигантоклеточная: озлокачествленная гигантоклеточная;
- онкообразования хорды — саркоматоидная хордома.
Стромальная — это опухоль развивается чаще всего матке и характерна для эндометрия. Частой причиной ее возникновения является облучение. Также причиной этого вида саркомы могут быть аборты и повреждения при родах, полипозы. Заболевание может проявляться болями и кровотечениями.
Веретеноклеточная. Этот вид опухоли состоит из веретенообразных структур. Требуется дифференцировка с фибромой. Узлы этой опухоли плотные и волокнистые по структуре и чаще располагаются на коже, слизистых, фасции и серозных покровах. Выявленная на ранних этапах эта опухоль имеет благоприятный прогноз.

Злокачественная — это мягкотканое образование, имеет высокий процент рецидива (свыше 40%), обычно располагается глубоко в мышечных тканях. На начальных стадиях заболевание развивается бессимптомно.
Плеоморфная. Такой вид заболевания обычно развивается в конечностях (голени, пальцах рук или ног), на туловище — значительно реже. Выявляется такая опухоль чаще лишь, когда дорастает до крупных размеров (больше 10 см). Выглядит эта опухоль как образование с плотной дольчатой структурой, которая содержит зоны кровоизлияний мертвых тканей. Для этого вида саркомы характерна низкая выживаемость пациентов – около 10%.
Полиморфноклеточная относится к первичным кожным, которые формируются по мягкотканой периферии. При разрастании такого вида саркомы изъявляются, дают метастазы лимфогенным путем. Лечатся только путем хирургического вмешательства.
Недифференцированная. Хотя такой вид саркомы тяжело отнести к какому-либо классу, она относится к опухолям неясной тканевой принадлежности, но лечат ее как рабдомиосаркому.
Гистиоцитарная опухоль имеет клетки полиморфной структуры. Этот вид заболевания имеет неблагоприятный прогноз. Чаще всего поражает мягкотканные структуры, органы ЖКТ. При лечении негативно реагирует на терапевтическое воздействие.

Круглоклеточная. Этот вид саркомы содержит круглые клеточные структуры, считается высоко злокачественной опухолью, распространяется в мягкотканные структуры и клетки кожи.
Фибромиксоидная является низкозлокачественной, может диагностироваться у пациентов любого возраста. Располагается, как правило, на бедрах, плечах, туловище. Данный вид опухоли растет медленно, практически не дает метастаз.
Лимфоидная поражает иммунные структуры и имеет полиморфную симптоматику. Для нее характерно увеличение лимфоузлов, аутоиммунная анемия, экземоподобные поражения кожи. Опухоль может сдавливать сосуды, чем провоцирует появление некроза.
Эпителиоидная чаще всего поражает конечности, в основном у молодых пациентов. Это новообразование относится к разновидностям синовиальной саркомы.
Миелоидная саркома состоит из миелобластов лейкозного типа, чаще всего располагается в костях черепной коробки, внутриорганических структурах, лимфатических узлах.
Светлоклеточная — фасциогенное образование, располагается в зоне головы, шеи, туловища, распространяется в мягкотканные структуры, растет медленно, дает метастазы, часто рецидивирует.
Нейрогенная формируется чаще всего на ногах, медленно развивается, имеет клетки веретенообразного типа, ограничивается от других тканей. Терапия — исключительно хирургическое вмешательство, прогнозы — благоприятные. Выживаемость — около 80%.
Для стадирования ОССЮ используется 6-ая версия TNM классификации (Международной классификации злокачественных опухолей). (Таблица 2) Для определения стадии заболевания, следует придерживаться общих правил, применяемых для всех локализаций злокачественных опухолей, а именно:
- Во всех случаях должно быть гистологическое подтверждение диагноза;
- Описываются две классификации:
- клиническая (TNM) применяется до начала лечения, которая основывается на данных всех доступных методов обследования, данных биопсии и хирургических способах исследования;
- патологическая классификация (постхирургическая, патогистологическая), которая обозначается pTNM, основанная на данных, полученных до начала лечения, но дополненных или измененных на основании сведений, полученных при хирургическом вмешательстве или патоморфологическом исследовании операционного материала.
- На основании данных TNM или рТ pN рМ производится группировка по стадиям;
- При сомнениях в правильности определения категории TNM — надо выбирать низшую (т. е. менее распространенную) категорию;
- При тотальном поражении кости или практически на протяжении всего длинника кости, или при поражении соседних костей, выставляется T3.
Таблица 2 – Классификация TNM
| Первичная опухоль (Тumor) | |
| Тх | Размер первичной опухоли не был определен |
| T0 | Отсутствие данных о первичной опухоли |
| T1 | Наибольший размер опухоли ? 8 см |
| T2 | Наибольший размер опухоли {amp}gt;8 см |
| T3 | Несколько несвязанных опухолей в первичной зоне поражения кости |
| Регионарные лимфоузлы (Nodus) | |
| Nx | Исследование регионарных лимфоузлов не проводилось |
| N0 | Нет данных о поражении регионарных лимфоузлов |
| N1 | Поражение регионарных лимфоузлов |
| Отдаленные метастазы (Мetastasis) | |
| Mx | Исследование для выявления отдаленных метастазов не проводилось |
| M0 | Нет данных об отдаленных метастазах |
| M1 | Отдаленные метастазы |
| M1a | в легких |
| M1b | другие локализации |
Таблица 3 – Гистологическое стадирование
| Gx | исследование не проводилось |
| G1 | хорошо дифференцированная |
| G2 | умеренно дифференцированная |
| G3 | плохо дифференцированная |
| G4 | недифференцированная |
Надо отметить, что для опухолей семейства саркомы Юинга характерна только высокозлокачественная (G3 и G4) степень дифференцировки.
Таблица 4 – Стадирование
| Стадия | TNM | Злокачественность (G) |
| Стадия IA | T1N0M0 | низкозлокачественная |
| Стадия IB | T2N0M0 | низкозлокачественная |
| Стадия IIA | T1N0M0 | высокозлокачественная |
| Стадия IIB | T2N0M0 | высокозлокачественная |
| Стадия III | T3N0M0 | любая G |
| Стадия IVA | любая T, N0, M1a | любая G |
| Стадия IVB | любая Т, N0, М1b любая T, N1, любая M | любая G любая G |
Приложение Г3. Контрольные обследования на этапе диспансерного наблюдения (после достижения ремиссии)
- Рекомендовано обратить внимание на наличие стрий, гиперпигментаций [2,4].
| Методы исследования | Сроки контрольных обследований, мес. | |||||||
| 3 | 6 | 9 | 12 | 15 | 18 | 21 | 24 | |
| ОАК, Б/Х (с определением уровня ЩФ, ЛДГ) | X | X | X | X | X | X | ||
| КТ органов грудной клетки | X | X | X | X | X | X | X | X |
| Рентгенография области первичного опухолевого очага | X | X | X | X | X | X | X | X |
| Радиоизотопное исследование костной системы и мягких тканей | X | X | X | X | ||||
| УЗВТ регионарных лимфатических узлов, органов брюшной полости, области первичного опухолевого очага | X | X | X | X | X | X | X | X |
| Консультация детского онколога | X | X | X | X | X | X | X | X |
2.5 Иная диагностика
- Рекомендуется биопсия опухоли для определения гистогенеза. [8,15].
Уровень убедительности B (уровень доказательности 2а)
Саркома Юинга — радиочувствительная опухоль. Лучевую терапию проводят пациентам, имеющим частичный или полный эффект после проведения индукционной терапии.
- Облучение первичного очага рекомендуется проводить после 4-5 курса ПХТ [4].

Уровень убедительности C (уровень доказательности -4).
Интенсивная химиотерапия (CEVAIE) состоит из 9 чередующихся курсов ифосфамида, винкристина, актиномицина D (I3VA); карбоплатина, эпирубицина, винкристина (CEV); и ифосфамида, винкристина, этопозида (I3VE). Интервал между курсами составляет 3 недели, а общая продолжительность интенсивной химиотерапии – 25 недель.
Курс I3VA: Ифосфамид (IFO): 3000 мг/м2 ифосфамида вводится в виде 3-часовой в/в инфузии в дни 1, 2 и 3 каждого курса I3VA. Параллельное введение месны 3000 мг/м2/сут до момента времени через 12-48 ч после окончания инфузии IFO. 20% всей дозы месны должно даваться в виде начального болюсного введения.
Рекомендуется гидратация по меньшей мере 3000 мл/м2/сут, начиная за 3 часа до и заканчивая через 24-48 ч после введения IFO.Винкристин (VCR): 1.5 мг/м2 винкристина вводится в виде единичной болюсной инъекции в день 1 каждого курса I3VA (максимальная разовая доза 2 мг). Курс 1: интенсификация благодаря дополнительному введению 1.
Курс терапии I3VA
| День | Ифосфамид | Винкристин | Актиномицин D | Месна | Дата |
| 1 | 3000 мг/м2 | 1.5 мг/м2 в/в болюс | 1.5 мг/м2 в/в болюс | 3000 мг/м2 | |
| 2 | 3000 мг/м2 | 3000 мг/м2 | |||
| 3 | 3000 мг/м2 | 3000 мг/м2 | |||
| 8 | 1.5 мг/м2 в/в болюс Только курс 1! | ||||
| 15 | 1.5 мг/м2 в/в болюс Только курс 1! | ||||
| Итого | 9000 мг/м2 | 4.5 мг/м2 (курс 1) 1.5 мг/м2 (курсы 4 и 7) | 1.5 мг/м2 |
Карбоплатин (CARBO): 500 мг/м2 карбоплатина в 200 мл/м2 5% раствора декстрозы вводится в виде 1-часовой в/в инфузии в день 1 каждого курса CEV.Эпирубицин (EPI): 150 мг/м2 эпирубицина в 5% растворе декстрозы вводится в виде 6-часовой в/в инфузии в день 1 каждого курса CEV – после введения карбоплатина.
Курс терапии CEV
| День | Карбоплатин | Эпирубицин | Винкристин | Дата |
| 1 | 500 мг/м2 в/в | 150 мг/м2 | 1.5 мг/м2 в/в болюс | |
| 8 | 1.5 мг/м2 в/в болюс Только курс 2! | |||
| 15 | 1.5 мг/м2 в/в болюс Только курс 2! | |||
| Итого | 500 мг/м2 | 150 мг/м2 | 4.5 мг/м2 (курс 2) 1.5 мг/м2 (курсы 5 и 8) |
:Ифосфамид (IFO): 3000 мг/м2 ифосфамида вводится в виде 3-часовой в/в инфузии в дни 1, 2 и 3 каждого курса I3VE. Параллельное введение месны 3000 мг/м2/сут до момента времени через 12-48 ч после окончания инфузии IFO. 20% всей дозы месны должно даваться в виде начального болюсного введения. Рекомендуется гидратация по меньшей мере 3000 мл/м2/сут, начиная за 3 часа до и заканчивая через 24-48 ч после введения IFO.
Курс терапии I3VE
| День | Ифосфамид | Винкристин | Этопозид | Месна | Дата |
| 1 | 3000 мг/м2 | 1.5 мг/м2 в/в болюс | 150 мг/м2 в/в | 3000 мг/м2 | |
| 2 | 3000 мг/м2 | 150 мг/м2 в/в | 3000 мг/м2 | ||
| 3 | 3000 мг/м2 | 150 мг/м2 в/в | 3000 мг/м2 | ||
| Итого | 9000 мг/м2 | 1.5 мг/м2 | 450 мг/м2 |

По поводу интратекальной химиотерапии в случае параменингеальных опухолей с распространением опухолевых клеток в цереброспинальную жидкость (ЦСЖ) см. раздел с тиотепой далеее.
Пероральную поддерживающую терапию ОТIЕ · (Trofosfamide / Idarubicine / Etoposid)Пероральную поддерживающую терапию еще на пол года может быть предоставлено после 3-х циклов CEVAIE и местной терапии пациентам c частичной регрессией. Состоит из периодических применений Трофосфамид Идарубицина с Трофосфамид Этопозид.
Максимум 8 курсов (продолжительностью 3 недели) может быть применена с общей продолжительностью терапии 24 недели.Физические и лабораторные исследования до начала обслуживания:· тщательное физическое обследование;· полный анализ крови (включая дифференциальный подсчет лейкоцитов и тромбоцитов);
· отсутствие беременности, отсутствие кормления грудью;· хорошее общее клиническое состояние пациента;· нет мукозита;· отсутствие инфекционных признаков и отсутствием лихорадки, как минимум, в течение 3 дней после последнего заражения;· отсутствие каких-либо соответствующих дисфункций органов (особенно почки, печень, сердце и ЦНС);
План лечения на пероральную поддерживающую терапиюКурс OT-I:Трофосфамид (ТРО): 150 мг/м2 Trofosfamide в день перорально, разделенные на 2 дозы/д от 1 дня до 10.Идарубицин (МАТ): 5 мг/м2 Idarubicine в день перорально, один раз утром в дни 1, 4, 7 и 10.
Курс OT-Е:(ТРО): 150 мг/м2 Trofosfamide в день перорально, разделенные на 2 дозы/д от 1 дня до 10.Etoposid (ето): 50 мг/м2 Etoposid в день перорально, разделенные на 2 дозы/д от 1 дня до 10.
После двух курсов карбоплатина/этопозида проводится один курс ифосфамида/этопозида. Впоследствии проводится третий курс карбоплатина/этопозида. Лечение завершается двумя курсами карбоплатина/ифосфамида.Условия начала химиотерапии соответствуют общим рекомендациям.План лечения для терапии второй линии▲повторная радиологическая оценка опухоли.

● BMA = аспирация костного мозга.Курс AКарбоплатин (CARBO): 150 мг/м2/сут карбоплатина вводится в виде 1-часовой в/в инфузии в дни 1, 2, 3 и 4. Гидратация 3000 мл/м2/сут и замещение электролитов.Этопозид (ETO): 150 мг/м2/сут этопозида вводится в виде 1-часовой в/в инфузии в дни 1, 2, 3 и 4. Гидратация 3000 мл/м2/сут и замещение электролитов.
Ифосфамид (IFO): 2000 мг/м2 ифосфамида вводится в виде 3-часовой в/в инфузии в дни 1, 2, 3 и 4. Параллельное введение месны3000 мг/м2/сут до момента времени 48 ч после окончания инфузии IFO. 20% всей дозы месны должно даваться в виде начального болюсного введения. Рекомендуется гидратация по меньшей мере 3000 мл/м2/сут, начиная за 3 часа до и заканчивая через 48 ч после введения IFO.Этопозид (ETO): 150 мг/м2/сут этопозида вводится в виде 1-часовой в/в инфузии в дни 1, 2, 3 и 4. Гидратация 3000 мл/м2/сут и замещение электролитов.
Курс CКарбоплатин (CARBO): 150 мг/м2/сут карбоплатина вводится в виде 1-часовой в/в инфузии в дни 1, 2, 3 и 4. Гидратация 3000 мл/м2/сут и замещение электролитов.Ифосфамид (IFO): 2000 мг/м2 ифосфамида вводится в виде 3-часовой в/в инфузии в дни 1, 2, 3 и 4. Параллельное введение месны 3000 мг/м2/сут до момента времени 48 ч после окончания инфузии IFO.
ВАРИАНТ ВТОРОЙ ЛИНИИ ТЕРАПИИПлохой ответ на первично проведенную химиотерапию часто соответствует плохому прогнозу у больных RMS.Режим Topo-Carbo
Режим Doxo – Carbo
Доксорубицин: 60 мг/м2/день, 1день (общая доза 60 мг/м2/курс) в течение1-6 часов. Карбоплатин: 250 мг/м2/день, 1 и 2 дни, (общая доза 500мг/м2/курс) в течение 1 часа.Циклофосфан: 1500 мг/м2/день, 1 и 2 дни, (общая доза 3000 мг/м2/курс) в течение 4 часов.Метрономная химиотерапия при саркомах мягких тканейЦиклофосфамид (Цикло) 2 x 25mg/m²/d x 14 день PO Mесна 50 mg/m²/ 0 {amp}amp; 4h) x 14 день POВинбластин (Винб) 3mg/m²/неделю IV
| Цикло | Цикло | Цикло | Цикло | |||||
| Meсна | Meсна | Meсна | Meсна | |||||
| Винб | Винб | Винб | Винб | |||||
| Дата | ||||||||
| Недели | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Цикло | Цикло | Цикло | Цикло | |||||
| Meсна | Meсна | Meсна | Meсна | |||||
| Винб | Винб | Винб | Винб | |||||
| Дата | ||||||||
| Недели | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| Цикло | Цикло | Цикло | Цикло | |||||
| Meсна | Meсна | Meсна | Meсна | |||||
| Винб | Винб | Винб | Винб | |||||
| Дата | ||||||||
| Недели | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
- Лечение пациентов с генерализованной стадией болезни рекомендовано начинать по одинаковой схеме с локализованной формой ОССЮ. На начальном этапе рекомендуется проводить индукционную/предоперационную ПХТ (полихимиотерапия), действие которой направлено на сокращение размеров первичной опухоли и регрессию отдаленных метастазов у пациентов с диссеминированными стадиями заболевания. Предоперационная ПХТ используется с расчётом на хороший клинический эффект. Это позволяет осуществить резекцию опухоли и вовлечённых в процесс мягких тканей [4].
Уровень убедительности C (уровень доказательности -4)
- Рекомендуется применение следующих схем индукционной/предоперационной ПХТ вне зависимости от стадии заболевания и группы риска: гиперVAC/IE в альтернирующем режиме (4-5 курсов).
hrVAC:
- Винкристин** 1,5 мг/м2 (не более 2 мг), в/в, стр., в 1-й, 8-й, 15-й день;
- Доксорубицин** 75 мг/м2/курс в/в кап. в виде 24 часовой инфузии, в 1-й и 2-й день;
- Циклофосфамид 2100 мг/м2 1-2 день, в/в кап. в течение 4 часов, на фоне уромитексана.
https://www.youtube.com/watch?v=e8DnYo8ELwo
hr IE:
- Этопозид** 100 мг/м2 в/в, кап. в 1–5 дни;
- Ифосфамид** 2400 мг/м2 в/в, кап. в течение 4-6 часов, в 1–5 дни на фоне уромитексана
3.2 Хирургическое лечение
- В случае возможности выполнения радикальной операции рекомендуется выполнение эндопротезирования пораженных костей и суставов.
- В случае, если возраст пациентов младше 14-15 лет (зоны роста скелета закрыты), рекомендуется использование раздвижного эндопротеза с неинвазивным механизмом роста.
- Хирургический этап, в случае резектабельности опухоли, рекомендовано выполнить после 4-5 курса предоперационной ПХТ.
- При лечебном патоморфозе III-IV степени рекомендовано продолжить ХТ в группе стандартного риска по вышеприведенным схемам VAC/IE [4].
Уровень убедительности А (уровень доказательности -1а)




